作者:河北广盾科技有限公司
在肿瘤治疗的漫长征程中,抗体偶联药物(ADC)的问世被誉为“生物导弹”的突破。这类药物通过将靶向肿瘤抗原的单克隆抗体与高效细胞毒性药物(有效载荷)精巧结合,实现了对癌细胞的精准打击,在乳腺癌、胃癌、淋巴瘤等多种癌症治疗中取得了令人瞩目的成就。然而,与许多抗癌药物一样,耐药性的出现仍然是临床上面临的一大挑战。当ADC药物疗效下降或失效时,患者和家属难免感到焦虑与迷茫。本文旨在科学解读ADC耐药的机制,系统介绍后续治疗的策略与方向,并赋予大家与疾病长期共存的信心。
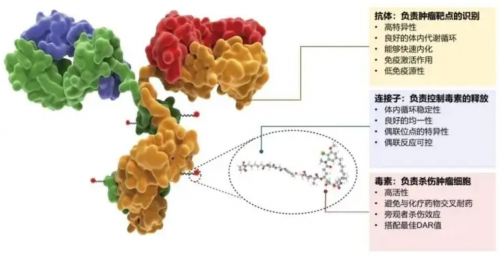
图|抗体偶联药物的结构及各部分功能
一、 ADC药物耐药的复杂机制
要理解如何应对耐药,首先需要知道耐药是如何发生的。ADC药物的作用是一个多步骤的精密过程,包括:与肿瘤细胞表面特异性抗原结合、内吞进入细胞、在溶酶体内被切割或降解、释放出有效载荷、最后有效载荷发挥作用导致细胞死亡。这个链条上的任何一个环节出现故障,都可能导致耐药。目前研究发现,耐药机制主要分为以下几类:
靶点抗原相关改变:这是最常见的原因之一。肿瘤细胞表面ADC所靶向的抗原表达水平可能下调甚至完全消失,使得ADC药物“找不到”目标而无法结合。例如,在使用靶向HER2的ADC治疗过程中,部分肿瘤细胞会通过表观遗传改变或信号通路反馈,减少HER2蛋白在细胞膜上的表达。此外,抗原表位也可能发生突变,导致抗体识别能力下降。
内吞及细胞内转运障碍:ADC与抗原结合后,需要依赖细胞的内吞作用进入细胞内。肿瘤细胞可能改变内吞途径的效率,或干扰ADC-抗原复合物向溶酶体的运输,使其无法到达“释放车间”,有效载荷也就无法被解放出来。
溶酶体功能障碍:溶酶体是ADC药物释放有效载荷的关键场所。肿瘤细胞可能通过降低溶酶体内蛋白酶(如组织蛋白酶)的活性,或改变溶酶体的酸度(pH值),影响连接子(连接抗体和有效载荷的化学键)的切割,导致“导弹”无法卸下“弹头”。
有效载荷耐药:有效载荷(通常是化疗药物,如微管蛋白抑制剂或DNA损伤剂)被释放后,肿瘤细胞可能通过多种经典的化疗耐药机制来对抗它。例如,上调药物外排泵蛋白(如P-糖蛋白),将细胞内的毒素“泵出”细胞外;或改变药物作用的靶点(如微管蛋白亚型),降低其敏感性;增强DNA修复能力等。
旁路激活与信号代偿:肿瘤细胞具有强大的进化与适应能力。当ADC药物抑制了其主要依赖的信号通路后,细胞可能激活其他平行的或下游的信号通路来维持生存和增殖,实现“绕道而行”。
肿瘤微环境影响:肿瘤并非孤立的细胞团,它存在于一个复杂的微环境中。其中的成纤维细胞、免疫细胞等可能分泌各种因子,间接保护肿瘤细胞,削弱ADC药物的效果。
理解这些机制并非为了增加忧虑,而是为了让我们明白,耐药是肿瘤细胞在生存压力下“进化”的结果,是一个可被研究和干预的科学问题。每一种耐药机制背后,都对应着科学家们正在探索的破解之道。
二、 耐药后的治疗策略与选择
当出现ADC药物耐药时,并不意味着治疗走到了尽头。相反,现代肿瘤医学已经发展出多层次、序贯化的治疗策略。医生会根据耐药的可能机制、患者的具体情况(如肿瘤类型、既往治疗史、身体状况等)来制定个体化的后续方案。
策略一:优化现有ADC治疗方案
在患者耐受性允许的情况下,经医生严谨评估,适当调整ADC药物的剂量或给药方案,有时可能克服部分因药物暴露不足导致的早期耐药。如果耐药主要与特定的有效载荷(如某种微管蛋白抑制剂)相关,换用搭载不同作用机制有效载荷(如DNA损伤剂)的同类靶点ADC,可能重新获得疗效。例如,从搭载美登木素生物碱衍生物的ADC,换为搭载依沙替康衍生物的ADC,为患者提供了新的攻击武器。
策略二:转向其他靶点的ADC或新型ADC
肿瘤细胞表面往往不止表达一种抗原。当原靶点抗原下调时,可以转向靶向其他肿瘤相关抗原的ADC药物。例如,在乳腺癌治疗中,除了HER2,还有Trop-2、HER3等多种靶点ADC正在临床应用或研发中,为患者提供了“换靶射击”的机会。此外,新一代ADC技术,如双特异性ADC(能同时结合两个靶点)、免疫刺激ADC(在杀伤肿瘤细胞的同时激活免疫)等,也正在临床试验中展现出克服耐药的潜力。
策略三:联合治疗——构建多维攻击网络
ADC与靶向药联合:联合使用作用于不同信号通路的小分子靶向药物。例如,将ADC与PI3K抑制剂、mTOR抑制剂或CDK4/6抑制剂联用,可以阻断肿瘤细胞的代偿性信号通路,起到协同增效的作用。
ADC与免疫治疗联合:ADC药物在杀死肿瘤细胞时,可能导致肿瘤抗原释放,改变免疫微环境,与免疫检查点抑制剂(如PD-1/PD-L1抑制剂)联用,有可能将“冷肿瘤”变为“热肿瘤”,激发患者自身的免疫系统来攻击癌症,形成长效控制。
ADC与化疗/抗血管生成药联合:与传统化疗或抗血管生成药物联合,可以从不同机制协同攻击肿瘤细胞和其赖以生存的血管网络。
双ADC联合:在特定情况下,联合使用两种不同靶点或不同有效载荷的ADC,也是一种探索中的策略。
三、 信心与希望:科学与患者同行
首先,耐药是治疗过程中的常见挑战,而非终点。正如细菌对抗生素会产生耐药一样,肿瘤细胞在药物压力下发生进化是其生物学特性使然。这恰恰说明了治疗是有效的,迫使肿瘤细胞做出了改变。现代肿瘤学的进步,正是与肿瘤细胞的这种“进化”进行的一场智慧博弈。
其次,治疗选择正在以前所未有的速度增长。过去十年是ADC药物爆发的“黄金十年”,而下一个十年,我们将见证更多更智能、更强大的抗癌武器问世。除了ADC,还有双抗、细胞治疗、癌症疫苗、溶瘤病毒等多种新模态疗法在飞速发展。针对各种耐药机制的破解策略,正是全球科学家和临床医生研究的焦点。
第三,“慢性病管理”理念日益深入。随着治疗手段的丰富,许多晚期癌症正在向“可控可治的慢性病”转变。治疗的目标是长期控制肿瘤,提高生活质量,延长生存期。即使出现耐药,通过序贯、轮换或联合使用不同的治疗手段,很多患者可以实现与肿瘤的长期共存。
结语
ADC药物耐药的出现,是抗癌路上的一道沟壑,但绝非不可逾越的悬崖。它揭示着肿瘤的狡猾,更激励着科学的奋进。通过深入理解耐药机制,我们拥有了更清晰的应对地图;通过不断涌现的后续治疗策略,我们拥有了更多元化的武器选择。在这场持久的斗争中,信心来源于对科学发展的认知,也来源于医患携手、步步为营的实践。请相信,每一次挑战的到来,都伴随着新的希望与突破的可能。前路虽漫,行者必至。(完)